5.8 尼克酸
5.8.1 结构与性质
尼克酸亦名烟酸,具有生理活性的衍生物为尼克酰胺,亦名烟酰胺(nicotinamide),结构式如图5-23。尼克酸为不吸水的较稳定的白色结晶,在230℃升华,能溶于水及溶于水及酒精中,25℃时,1g能溶于60ml水或80ml酒精中,不溶于乙醚中。尼克酸很容易变成尼克酰胺,它比尼克酸更易溶解,1g可溶于1ml水或1.5ml酒精中,在乙醚中也能溶解。
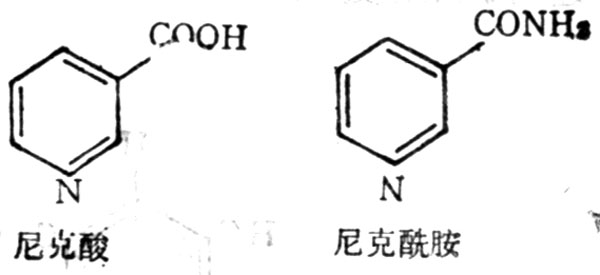
图5-23 尼克酸尼克酰胺结构式
5.8.2代谢
尼克酰胺通过ATP作用形成NAD或NADP。在尿中排出的尼克酰胺甚少,主要排出其代谢产物N‘-甲尼克酰胺及N’甲-2吡酮-5-甲酰胺。前者约占正常人的排出量的20~30%,后者为40~60%。血清中尼克酰胺含量甚微,仅为0.5μg・ml-1,红、白细胞中含量较多,全血为30μg・ml-1,红细胞为90μg・ml-1,白细胞为70μg・ml-1。
5.8.3生理功能
尼克酰胺为辅酰Ⅰ及辅酶Ⅱ的组成成分。辅酶Ⅰ为尼克酰胺腺嘌呤二核苷酸(NAD+或DPN+),辅酶Ⅱ为尼克酰胺腺嘌呤二核苷酸磷酸(NADP+或TPN+)(图5-24)。它们都是脱氢酶的辅酶,氢的传递通过在尼克酰胺4位上增加一个氢原子。在立体上又分为A、B二个部位,某些尼克酰胺脱氢酶具有立体专一性(图5-25)。其立体专一性表现为两个方面:一方面只对一种立体异构体的底物有催化作用,如乳酸脱氢酶脱氢酶只作用于乳酸。另一方NAD+或NAP+被酶还原时,氢原子只在一个特定的方向加到吡啶环的第四位碳原子上,有的加到A侧,有的加到B侧。
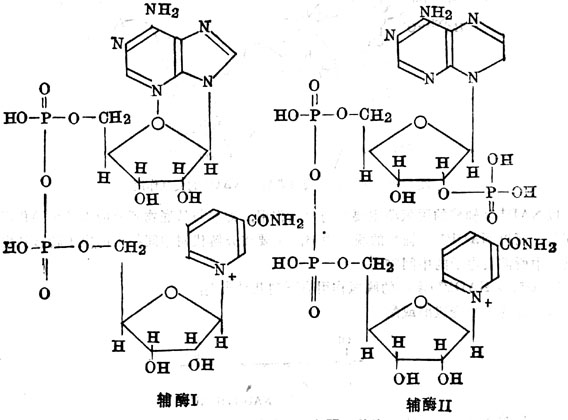
图5-24 辅酶Ⅰ及Ⅱ的结构
需要辅酶Ⅰ、Ⅱ的脱氢酶有数百种,这些脱 氢酶从底物中提取一个氢,二个电子,其结构通过X光衍射图看出脱氢酶与NAD+及底物的结构。图5-26表明乳酸脱氢酶与NAD+及底物的关系。底物乳酸给NAD+一个H,底物的羟基与酶的精氨酸(171)的胍基相连,而在组氨酸(195)中OH基中提取一个质子。其他脱氢酶的构象与之相同。

图5-25 尼克酰胺4位C上联结H的主体构造:A,B二个位置
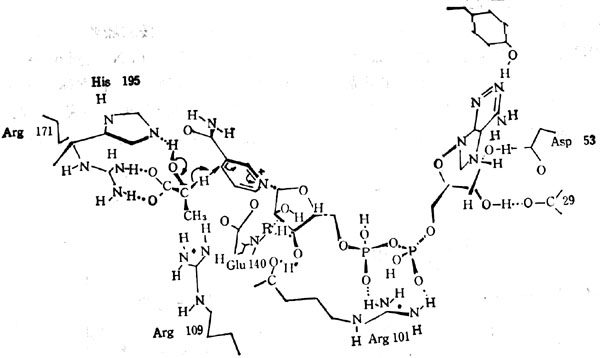
图5-26 乳酸脱氢酶乳酸及NAD+的交互作用
以NAD+为辅酶的脱氢酶主要参与呼吸作用,即参与从底物到氧的电子传递作用的中间环节。而以NADP+为辅酶脱氢酶类,主要将分解代谢中间物上的电子转移到生物合成反应中所需要电子的中间物上。
NAD+(或NADP+)参与的脱氢作用下列几种类型:
(1) 底物由醇变成醛或酮

(2) 加阴离子A-到醛而脱氢

谷氨酸脱酶是谷氨酸脱氨的第一步,形成α-亚氨基戊二酸。
谷氨酸 α-亚氨基戊二酸 α-酮戊酸

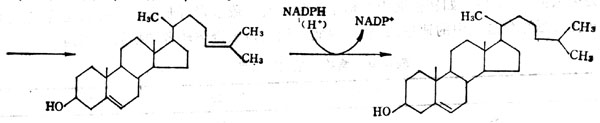
(4)由不饱和合键(――C――C――)到饱和键。由7-脱氢胆固醇转变为胆固醇,7α-H+从NADPH而来,而8β氢从介质而来。在胆固醇合成中,固醇载体蛋白将在胞液中形成的鲨烯转运至微粒体环化成羊毛脂固醇,再转变为链固醇。链固醇转变为胆固醇需要由NADPH供给25位氢,从介质中供给24位H+。
链固醇(又名24-脱氢胆固醇 胆固醇
(5)二硫键转为二硫醇键;许多酶催化这个反应,辅酶Ⅰ、Ⅱ为H+的供体或受体。如胱氨酸还原酶的作用为NADH2+1-胱氨酸→NAD+C+2-半胱酸。麦胱甘肽还原酶的作用为NAD(P)――H2氧化麦胱甘肽→NAD(P)+2G还原型麦胱甘肽。
在α-酮酸脱氢酶系统中,硫辛酸脱氢酶通过NADPH+与黄素蛋白作用,将H转移。
(6)苯丙氨酸通过苯氨酸4-单加氧酶(即苯氨酸羧化酶)的作用,变成酪氨酸。这个酶可作为单加氧酶可作为单加氧酶或混合功能加氧酶的代表,它的作用是将氧分子中的一个氧原子加到苯丙氨酸上形成对羧基,另一个氧原子还原成水。还原剂是NADPH,反应分两步进行:
NADPH+H++二氢生物蝶呤→NADPH++四氢生物蝶呤。

图5-27 色氨酸转变为尼克酸的途径
1-苯丙氨酸+四氢生物蝶呤+O2→1-酪氨酸+二氢生物蝶呤+H2O。
5.8.4 来源
尼克酸或尼克酰胺的来源除食物含有者外,尚可由色氨酸在体内转变为酰犬尿氨酸到犬尿氨酸,再由1-犬尿酸水解酶分解犬尿酸或黄尿酸为3-羧氨基苯四酸,然后在5磷酸核糖焦磷酸存在下,由哺乳类肝的酶系统变成尼克酸。一般说来,60mg色氨酸相当于1mg尼克酸。食物中尼克酸的当量为尼克酸及色氨酸转换为尼克酸之和(表5-16)。但转换能力因人而异,晚期孕妇转换能力3倍于正常妇女。雌激素可刺激色氨酸氧化酶,它是色氨酸转为尼克酸过程中的速率限制酶,因此孕妇及口服药者转换能力较强。
表5-16食物中尼克酸当理(mg・1000Kj-1)
| |
尼克酸 |
色氨酸 |
尼克酸当量 |
| 牛奶 |
5.08 |
283 |
|
| 人乳 |
10.3 |
1681 |
32.1 |
| 牛肉 |
103.7 |
5376 |
193 |
| 全蛋 |
2.5 |
4830 |
45.4 |
| 腌猪肉 |
4.8 |
256 |
11 |
| 面粉 |
10.4 |
1247 |
32 |
| 玉米渣 |
7.7 |
294 |
13 |
| 玉米 |
21 |
445 |
28 |
谷类中有结合型的尼克酸,不能利用。可分为二种结合物:①与肽链(分子量12,000~13,000)结合;②与碳水化物结合成复合体(分子量为370)。麸皮中有这种结合型的尼克酸(niacytin),用碱提取(或碱水解)和谷物,其尼克酸测定值较酸性或中性提取液的高20%,谷类通过培育新品种可使色氨酸增加,也可使其成为尼克酸来源。我国已培育出高色氨酸品种的玉米可治疗尼克酸缺乏引起的瘌皮病。
大剂量的亮氨酸可使癞皮病发生。Jowar(一种食物)尼克酸及色氨酸量不少,但因亮氨酸量大,也可使癞皮病发生。在大鼠的酪蛋白饲料中,若增加亮氨酸,尿中吡啶-2-3-二羧酸增加,可能影响色氨酸向尼克酸的转变。正常人的正常膳食中增加亮氨酸可以增加尿中吡啶二羧酸,而四基尼克酸胺及-6吡啶酮的排出量减少。
5.8.5 需要量及临床应用
尼克酸供应量为27.7mg・100KJ-1。婴儿0~6个月为33.6 mg・100KJ-1,2/3来源于色氨酸,一般75g蛋白有尼克酸当量NE15mg,6个月~青年时期为27.7mg・100KJ-1,孕妇增加2mg,乳母增加4mg。
尼可酸缺乏症可用生理剂量治疗。尼克酸及尼克酸胺对治疗及预防癞皮病有相同效果,但在药理上及毒性上二者不完全相同。尼克酸3g以上有药理作用,可使血中胆固醇、β-脂蛋白及甘油三酯量减低。可能由于减少从脂肪组织中动员出来脂肪酸,而增加肌肉或心肌的肝糖原的利用。因此长期使用易有糖尿病,对肝不利。它能导致组胺的释放,可使血管扩张,脸红为主要的副作用。如果在给药前15min给以抗组胺药,可以抑制脸红。尼克酸可以增加血清尿酸水平,每日3g剂量长达5年,可以使血清尿酸超过8mg%。在大剂量时,尼克酸与尿酸竟争排出,由于血清尿酸增加,所以大剂量尼克酸摄取者易患急性痛风症。