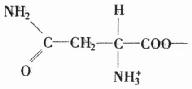
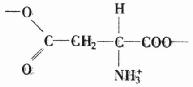
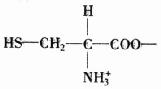
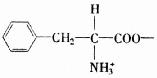
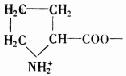
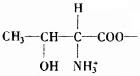
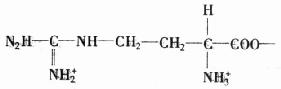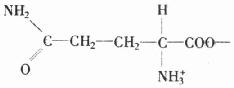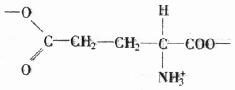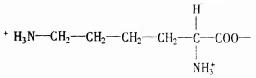ИНТМЫФЁЁЪЕбщЪвГЃгУММЪѕВЮЪ§зЪСЯ
вЛЁЂКЫЫсМАЕААзжЪГЃгУЪ§Он
1ЃЎ
| ЛЏКЯЮя | ЗжзгСП | ІЫmax(pH7.0) | 1ФІЖћШмвКЃЈpH7.0ЃЉжаІЫmaxЪБЕФзюДѓЮќЪежЕ | OD280/OD260 |
| ATP | 507 | 259 | 15400 | 0.15 |
| CTP | 483 | 271 | 9000 | 0.97 |
| GTP | 523 | 253 | 13700 | 0.66 |
| UTP | 484 | 262 | 10000 | 0.38 |
| dATP | 494 | 259 | 15200 | 0.15 |
| dCTP | 467 | 271 | 9300 | 0.98 |
| dGTP | 507 | 253 | 13700 | 0.66 |
| dTTP | 482 | 267 | 9600 | 0.71 |
2ЃЎГЃгУКЫЫсЕФГЄЖШгыЗжзгСП
| КЫЫс | КЫмеЫсЪ§ | ЗжзгСП |
| ІЫDNA | 48502ЃЈЫЋСДЛЗзДЃЉ | 3.0ЁС107 |
| pBR322 | 4363ЃЈЫЋСДЃЉ | 2.8ЁС106 |
| 28SrRNA | 4800 | 1.6ЁС106 |
| 23SrRNA | 3700 | 1.2ЁС106 |
| 18SrRNA | 1900 | 6.1ЁС105 |
| 19SrRNA | 1700 | 5.5ЁС105 |
| 5SrRNA | 120 | 3.6ЁС104 |
| tRNAЃЈДѓГІИЫОњЃЉ | 75 | 2.5ЁС104 |
3ЃЎГЃгУКЫЫсЕААзЛЛЫуЪ§Он
ЃЈ1ЃЉжиСПЛЛЫу
1ІЬg=10-6gЁЁ 1pg=10-12g
1ng=10-9g ЁЁ1fg=10-15g
ЃЈ2ЃЉЗжЙтЙтЖШЛЛЫуЃК
1A260ЫЋСДDNA=50ІЬg/ml
1A260ЕЅСДDNA=30ІЬg/ml
1A260ЕЅСДRNA=40ІЬg/ml
ЃЈ3ЃЉDNAФІЖћЛЛЫуЃК
1ІЬg 100bp DNA=1.52pmol=3.03pmolФЉЖЫ
1ІЬg pBR322 DNA=0.36pmol
1pmol 1000bp DNA=0.66ІЬg
1pmol pBR322=2.8ІЬg
1kbЫЋСДDNAЃЈФЦбЮЃЉ=6.6ЁС105ЕРЖћЖй
1kbЕЅСДDNAЃЈФЦбЮЃЉ=3.3ЁС105ЕРЖћЖй
1kbЕЅСДRNAЃЈФЦбЮЃЉ=3.4ЁС105ЕРЖћЖй
ЃЈ4ЃЉЕААзФІЖћЛЛЫуЃК
100pmolЗжзгСП100ЃЌ000ЕААзжЪ=10ІЬg
100pmolЗжзгСП50ЃЌ000ЕААзжЪ=5ІЬg
100pmolЗжзгСП10ЃЌ000ЕААзжЪ=1ІЬg
АБЛљЫсЕФЦНОљЗжзгСП=126.7ЕРЖћЖй
ЃЈ5ЃЉЕААзжЪ/DNAЛЛЫуЃК
1kb DNA=333 ИіАБЛљЫсБрТыШнСП=3.7ЁС104MWЕААзжЪ
10ЃЌ000MWЕААзжЪ=270bp DNA
30ЃЌ000MWЕААзжЪ=810bp DNA
50ЃЌ000MWЕААзжЪ=1.35kb
100ЃЌ000MWЕААзжЪ=2.7kb DNA
4ЃЎГЃгУЕААзжЪЗжзгСПБъзМВЮееЮя
| ЃЈ1ЃЉИпЗжзгСПБъзМВЮее | ЃЈ2ЃЉжаЗжзгСПБъзМВЮее | ЃЈ3ЃЉЕЭЗжзгСПБъзМВЮее | |||
| МЁЧђЕААз | ЗжзгСП | СзЫсЛЏУИB | 97ЃЌ400 | ЬМЫсєћУИ | 31ЃЌ00 |
| МЁЧђЕААз | 212ЃЌ000 | ХЃбЊЧхАзЕААз | 66ЃЌ200 | ДѓЖЙУЕААзУИ | 21ЃЌ500 |
| ІТ-АыШщЬЧИЪУИB | 116ЃЌ000 | ЙШАБУИЭбЧтУИ | 55ЃЌ000 | вжжЦМС | ЁЁ |
| СзЫсЛЏУИB | 97ЃЌ400 | ТбАзЕААз | 42ЃЌ700 | ТэаФМЁЧђЕААз | 16ЃЌ900 |
| ХЃбЊЧхАзЕААз | 66ЃЌ200 | ШЉЫѕУИ | 40ЃЌ000 | ШмОњУИ | 14ЃЌ400 |
| Й§бѕЛЏЧтУИ` | 57ЃЌ000 | ЬМЫсєћУИ | 31ЃЌ000 | МЁЧђЕААзЃЈF1ЃЉ | 8ЃЌ100 |
| ШЉЫѕУИ | 40ЃЌ000 | ДѓЖЙУЕААзУИ | 21ЃЌ500 | МЁЧђЕААзЃЈF2ЃЉ | 6ЃЌ200 |
| ЁЁ | ЁЁ | вжжЦМС | ЁЁ | МЁЧђЕААзЃЈF3ЃЉ | 2ЃЌ500 |
| ЁЁ | ЁЁ | ШмОњУИ | 14ЃЌ400 | ЁЁ | ЁЁ |
5ЃЎГЃгУDNAЗжзгСПБъзМВЮееЮя
| ІЫDNA/HindЂѓ | ІЫDNA/EcoRЂё | ІЫ/HindЂѓ+EcoRЂё | pBR322/HaeЂѓ | |
| 23130 | 21226 | 21227 | 587 | 123 |
| 9416 | 7421 | 5148 | 405 | 104 |
| 6557 | 5804 | 4973 | 504 | 89 |
| 4361 | 5643 | 4268 | 458 | 80 |
| 2322 | 4843 | 3530 | 434 | 64 |
| 2027 | 3530 | 2027 | 267 | 57 |
| 564 | ЁЁ | 1904 | 234 | 51 |
| 125 | ЁЁ | 1584 | 213 | 21 |
| ЁЁ | ЁЁ | 1375 | 192 | 18 |
| ЁЁ | ЁЁ | 974 | 184 | 11 |
| ЁЁ | ЁЁ | 831 | 124 | 7 |
| ЁЁ | ЁЁ | 564 | ЁЁ | ЁЁ |
| ЁЁ | ЁЁ | 125 | ЁЁ | ЁЁ |
ајЩЯБэ
| pBR322/HinfЂё | ІеІж174/HinfЂё | ІеІж174/Hae Ђѓ | ІеІж174/TapЂё | |
| 1631 | 726 | 140 | 1353 | 2914 |
| 517 | 713 | 118 | 1078 | 1175 |
| 506 | 553 | 100 | 872 | 404 |
| 396 | 500 | 82 | 603 | 327 |
| 344 | 417 | 66 | 310 | 231 |
| 298 | 413 | 48 | 281 | 141 |
| 221 | 311 | 42 | 271 | 87 |
| 220 | 249 | 40 | 234 | 54 |
| 154 | 200 | 24 | 194 | 33 |
| 75 | 151 | ЁЁ | 118 | 20 |
| ЁЁ | ЁЁ | ЁЁ | 72 | ЁЁ |
ЖўЁЂГЃгУЛКГхвК
1ЃЎЗжзгПЫТЁГЃгУЛКГхвК
2ЃЎСзЫсЛКГхвК
ЃЈ1ЃЉ25ЁцЯТ0.1mol/LСзЫсМиЛКГхвКЕФХфжЦЁљ
| pH | 1mol/L K2HPO4(ml) | 1mol/L KH2PO4(ml) |
| 5.8 | 8.5 | 91.5 |
| 6.0 | 13.2 | 86.8 |
| 6.2 | 19.2 | 80.8 |
| 6.4 | 27.8 | 72.2 |
| 6.6 | 38.1 | 61.9 |
| 6.8 | 49.7 | 50.3 |
| 7.0 | 61.5 | 38.5 |
| 7.2 | 71.7 | 28.3 |
| 7.4 | 80.2 | 19.8 |
| 7.6 | 86.6 | 13.4 |
| 7.8 | 90.8 | 9.2 |
| 8.0 | 94.0 | 6.2 |
ЃЈ2ЃЉ25ЁцЯТ0.1mol/LСзЫсФЦЛКГхвКЕФХфжЦЁљ
| pH | 1mol/L Na2HPO4(ml) | 1mol/L NaH2PO4(ml) |
| 5.8 | 7.9 | 92.1 |
| 6.0 | 12.0 | 88.0 |
| 6.2 | 17.8 | 82.2 |
| 6.4 | 25.5 | 74.5 |
| 6.6 | 35.2 | 64.8 |
| 6.8 | 46.3 | 53.7 |
| 7.0 | 57.7 | 42.3 |
| 7.2 | 68.4 | 31.6 |
| 7.4 | 77.4 | 22.6 |
| 7.6 | 84.5 | 15.5 |
| 7.8 | 89.6 | 10.4 |
| 8.0 | 93.2 | 6.8 |
Ёљ:гУеєСѓЫЎНЋЛьКЯЕФСНжж1mol/LжќДцвКЯЁЪЭжС1000mlЃЌИљОнHenderson-HasselbalchЗНГЬМЦЫуЦфpHжЕЃК
pH=pKЁЏ+1g([жЪзгЪмЬх]/[жЪзгЙЉЬх])
дкДЫЃЌpKЁЏ=6.86(25Ёц)ЁЃ
3ЃЎЕчгОЛКГхвК
ВтађФ§НКМгбљЛКГхвК
98%ШЅРызгМзѕЃАЗ
10mol/L EDTA(pH8.0)
0.025%ЖўМзБНЧрFF
0.025%фхЗгРЖ
МзѕЃАЗЃКаэЖрХњКХЕФЪдМСМЖМзѕЃАЗЃЌЦфДПЖШЗћКЯЪЙгУвЊЧѓЃЌЮоаыдйНјааДІРэЁЃВЛЙ§ЃЌвЛЕЉТдГЪЛЦЩЋЃЌдђгІгУдкДХСІНСАшЦїЩЯНЋМзѕЃАЗгыDowex XG8ЛьКЯДВЪїжЌЙВЭЌНСАш1аЁЪБНјааШЅРызгДІРэЃЌВЂгУWhatman 1КХТЫжНЙ§ТЫ2ДЮЃЌШЅРызгМзѕЃАЗЗжзАГЩаЁЗнЃЌГфЕЊДцгк-70ЁцЁЃ
ГЃгУЕФЕчгОЛКГхвК
| ЛКГхвК | ЪЙгУвК | ХЈжќДцвКЃЈУПЩ§ЃЉ |
| Tris-ввЫсЃЈTAEЃЉ | 1ЁСЃК0.04mol/L Tris-ввЫс | 50ЁСЃК242gTrisМю |
| ЁЁ | 0.001mol/L EDTA | 57.1mlБљввЫс |
| ЁЁ | ЁЁ | 100ml 0.5mol/L EDTA(pH8.0) |
| Tris-СзЫсЃЈTPEЃЉ | 1ЁС:0.09mol/L Tris-СзЫс | 10ЁС:10gTrisМю |
| ЁЁ | 0.002mol/L EDTA | 15.5ml85%СзЫсЃЈ1.679g/mlЃЉ |
| ЁЁ | ЁЁ | 40ml 0.5mol/L EDTA(pH8.0) |
| Tris-Х№ЫсЃЈTBEЃЉa | 0.5ЁС0.045mol/L Tris-Х№Ыс | 5ЁСЃК54gTrisМю |
| ЁЁ | 0.001mol/L EDTA | 27.5Х№Ыс |
| ЁЁ | ЁЁ | 20ml 0.5mol/L EDTA(pH8.0) |
| МюадЛКГхвКb | 1ЁС:50mmol/L NaOH | 1ЁС:5ml 10mol/L NaOH |
| ЁЁ | 1mmol/L EDTA | 2ml 0.5mmol/L EDTA(pH8.0) |
| Tris-ИЪАБЫсc | 1ЁС:25mmol/L Tris | 5ЁС:15.1gTris |
| ЁЁ | 250mmol/L ИЪАБЫс | 94gмеАБЫсЃЈЕчгОМЖЃЉЃЈpH8.3ЃЉ |
| ЁЁ | 0.1% SDS | 50ml 10% SDS(ЕчгОМЖ) |
ЫЕУїЃК
ЂйTBEШмвКГЄЪБМфДцЗХКѓЛсаЮГЩГСЕэЮяЃЌЮЊБмУтетвЛЮЪЬтЃЌПЩдкЪвЮТЯТгУВЃСЇЦПБЃДц5ЁСШмвКЃЌГіЯжГСЕэКѓдђгшвдЗЯЦњЁЃ
вдЦЌЖМвд1ЁСTBEзїЮЊЪЙгУвКЃЈМД1ЃК5ЯЁЪЭХЈжќвКЃЉНјааЧэжЌЬЧФ§НКЕчгОЁЃЕЋ0.5ЁСЕФЪЙгУвКвбОпБИзуЙЛЕФЛКГхШнСПЁЃФПЧАМИКѕЫљгаЕФЧэжЌЬЧНКЕчгОЖМвд1ЃК10ЯЁЪЭЕФжќДцвКзїЮЊЪЙгУвКЁЃ
НјааОлБћЯЉѕЃАЗФ§НКДЙжБВлЕФЛКГхвКВлНЯаЁЃЌ ЙЪЭЈЙ§ЛКГхвКЕФЕчСїСПЭЈГЃНЯДѓЃЌашвЊЪЙгУ1ЁСTBEвдЬсЙЉзуЙЛЕФЛКГхШнСПЁЃ
ЂкМюадЕчгОЛКГхвКгІЯжгУЯжХфЁЃ
ЂлTris-ИЪАБЫсЛКГхвКгУSDSОлБћЯЉѕЃАЗФ§НКЕчгОЁЃ
2ЁСSDSФ§НКМгбљЛКГхвКЃК
100mmol/L TrisЁЄHCl(6.8)
200mmol/LЖўСђЫеЬЧДМЃЈDTTЃЉ
4%SDSЃЈЕчгОМЖЃЉ
0.2%фхЗгРЖ
20%ИЪгЭ
ВЛКЌDTTЕФ2ЁСSDSФ§НКМгбљЛКГхвКПЩБЃДцгкЪвЮТЃЌгІдкСйгУЧАШЁ1mol/LжќДцвКЯжМггкЩЯЪіЛКГхвКжаЁЃ
4ЃЎФ§НКМгбљЛКГхвК
| ЛКГхвКРраЭ | 6ЁСЛКГхвК | жќДцЮТЖШ |
| Ђё | 0.25%фхЗгРЖ | 4Ёц |
| 0.25%ЖўМзБНЧрFF | ||
| 40%ЃЈW/VЃЉесЬЧЫЎШмвК | ||
| Ђђ | 0.25фхЗгРЖ | ЪвЮТ |
| 0.25%ЖўМзБНЧрFF | ||
| 15%ОлесЬЧ(Ficoll400) | ||
| Ђѓ | 0.25%фхЗгРЖ | 4Ёц |
| 0.25%ЖўМзБНЧрFF | ||
| 30%ИЪгЭЫЎШмвК | ||
| Ђє | 0.25%фхЗгРЖ | 4Ёц |
| 40%(W/V)есЬЧЫЎШмвК | ||
| МюадМгбљЛКГхвК: | ||
| 300mmol/L NaOH | ||
| 6mmol/L EDTA | ||
| Ђѕ | 18%ОлесЬЧ(Ficoll400) | 4Ёц |
| 0.15%фхМзЗгТЬ | ||
| 0.25%ЖўМзБНЧрFF |
ЪЙгУвдЩЯФ§НКМгбљЛКГхвКЕФФПЕФгаШ§ЃКдіДѓбљЦЗУмЖШЃЛвдШЗБЃDNAОљдШНјШыбљЦЗПзФкЃЛЪЙбљЦЗГЪЯжбеЩЋЃЌДгЖјЪЙМгбљВйзїИќЮЊБуРћЃЌКЌгадкЕчПщжаФмвдПЩдЄжЊЫйТЪЯђбєМЋгОЖЏЕФШОСЯЁЃфхЗгРЖдкЧэжЌЬЧжавЦЖЏЕФЫйТЪдМЮЊЖўМзБНЧрFFЕФ2.2БЖЃЌЖјгыЧэжЌЬЧХЈЖШЮоЙиЁЃвд0.5ЁСTBFзїЕчгОвКЪБЃЌфхЗгРЖдкЧэжЌЬЧжаЕФгОЖЏЫйТЪдМгыГЄ300bpЕФЫЋСДЯпзДDNAЯрЭЌЃЌЖјЖўМзБНЧрFFЕФгОЖЏдђгыГЄ4kbЕФЫЋСДЯпзДDNAЯрЭЌЁЃдкЧэжЌЬЧХЈЖШЮЊ0.5%ЁЋ1.4%ЕФЗЖЮЇФкЃЌетаЉЖдгІЙиЯЕЪмФ§НКХЈЖШБфЛЏЕФгАЯьВЂВЛЯджјЁЃ
бЁгУФФвЛжжМгбљШОСЯДПЪєИіШЫЯВЖёЁЃЕЋЪЧЃЌЖдгкМюадФ§НКгІЕБЪЙгУфхМзЗгТЬзїЮЊЪОзйШОСЯЃЌвђЮЊдкМюадpHЬѕМўЯТЦфЯдЩЋНЯфхЗгИќРЖЮЊЯЪУїЁЃ
5ЃЎИїжжpHжЕЕФTrisЛКГхвКЕФХфжЦ
| ИїжжpHжЕЕФTrisЛКГхвКЕФХфжЦ | |
| ЫљашpHжЕЃЈ25ЁцЃЉ | 0.1mol/L HClЕФЬхЛ§ |
| 7ЃЎ1 | 45ЃЎ7 |
| 7ЃЎ2 | 44ЃЎ7 |
| 7ЃЎ3 | 43ЃЎ4 |
| 7ЃЎ4 | 42ЃЎ0 |
| 7ЃЎ5 | 40ЃЎ3 |
| 7ЃЎ6 | 38ЃЎ5 |
| 7ЃЎ7 | 36ЃЎ6 |
| 7ЃЎ8 | 34ЃЎ5 |
| 7ЃЎ9 | 32ЃЎ0 |
| 8ЃЎ0 | 29ЃЎ2 |
| 8.1 | 26.2 |
| 8.2 | 22.9 |
| 8.3 | 19.9 |
| 8.4 | 17.2 |
| 8.5 | 14.7 |
| 8.6 | 12.4 |
| 8.7 | 10.3 |
| 8.8 | 8.5 |
| 8.9 | 7.0 |
ФГвЛЬиЖЈpHжЕЕФ0.05mol/LTrisЛКГхвКЕФХфжЦЃКНЋ50ml 0.1mol/L TrisМюШмвКгыЩЯБэЫљЪОЯргІЬхЛ§ЃЈЕЅЮЛЃКmlЃЉЕФ0.1ml/L HClЛьКЯЃЌМгЫЎНЋЬхЛ§ЕїжС100ml
ЃЈ2ЃЉЮТЖШЖд50mmol/LTrisЁЄHClвКpHжЕЕФгАЯь
| 4Ёц | 25Ёц | 37Ёц |
| 8ЃЎ1 | 7ЃЎ5 | 7ЃЎ2 |
| 8ЃЎ2 | 7ЃЎ6 | 7ЃЎ3 |
| 8ЃЎ3 | 7ЃЎ7 | 7ЃЎ4 |
| 8ЃЎ4 | 7ЃЎ8 | 7ЃЎ5 |
| 8ЃЎ5 | 7ЃЎ9 | 7ЃЎ6 |
| 8ЃЎ6 | 8ЃЎ0 | 7ЃЎ7 |
| 8ЃЎ7 | 8ЃЎ1 | 7ЃЎ8 |
| 8ЃЎ8 | 8ЃЎ2 | 7ЃЎ9 |
| 8ЃЎ9 | 8ЃЎ3 | 8ЃЎ0 |
| 9ЃЎ0 | 8ЃЎ4 | 8ЃЎ1 |
| 9ЃЎ1 | 8ЃЎ5 | 8ЃЎ2 |
| 9ЃЎ2 | 8ЃЎ6 | 8ЃЎ3 |
| 9ЃЎ3 | 8ЃЎ7 | 8ЃЎ4 |
| 9ЃЎ4 | 8ЃЎ8 | 8ЃЎ5 |
ЃЈ6ЃЉГЃгУЛКГхвКЕФpKaжЕ
| ЛКГхвК | ЗжзгСП | pKaжЕ | ЛКГхЗЖЮЇ |
| Trisa | 12.1 | 8.08 | 7.1ЁЋ7.9 |
| HEPESb | 283.3 | 7.47 | 7.2ЁЋ8.2 |
| MPOSc | 209.3 | 7.15 | 6.6ЁЋ7.8 |
| PIPESd | 304.3 | 6.76 | 6.2ЁЋ7.3 |
| MESe | 195.2 | 6.09 | 5.4ЁЋ6.8 |
aЃКШ§єЧМзЛљАБЛљМзЭщЃЛbЃКN-2-єЧввЛљппрК-NЁЏ-2-ввСзЫсЃЛcЃК3-ЃЈN-Т№пјДњЃЉБћЛЧЫсЃЛdЃКNЃЌNЁЏ-ЫЋЃЈ2-ввЛЧЫсЃЉппрКЃЛeЃК2-ЃЈN-Т№пјДњЃЉввЛЧЫсЁЃ
7ЃЎЮТЖШЖдГЃгУЛКГхвКpHЕФгАЯь
| ЛКГхЬхЯЕ | pKa(20Ёц) | ЁїpKa/10Ёц |
| Mes | 6.15 | -0.110 |
| Ada | 6.60 | -0.110 |
| PiPes | 6.80 | -0.085 |
| Aces | 6.90 | -0.200 |
| Bes | 7.15 | -0.160 |
| Mops | 7.20 | -0.013 |
| Tes | 7.50 | -0.200 |
| Hepes | 7.55 | -0.014 |
| Tricine | 8.15 | -0.210 |
| Tris | 8.30 | -0.310 |
| Bicine | 8.35 | -0.180 |
| Glycylglycine | 8.40 | -0.280 |
Ш§ЁЂГЃгУУИЕФХфжЦ
1ЃЎШмОњУИ
гУЫЎХфжЦГЩ50mg/mlЕФШмОњУИШмвКЃЌЗжзАГЩаЁЗнВЂБЃДцгк-20ЁцЁЃУПвЛаЁЗнвЛОЪЙгУКѓБугшЖЊЦњЁЃ
2ЃЎЕААзЫЎНтУИРр
| ЁЁ | жќДцвК | жќДцЮТЖШ | ЗДгІХЈЖШ | ЗДгІЛКГхвК | ЮТЖШ | дЄДІРэ |
| 0.01mol/L Tris(pH7.8) | ||||||
| СДУЙЕААзУИa | 20mg/ml | -20ЁцЃЈШмгкЫЎЃЉ | 1mg/ml | 0.01mol/L EDTA | 37Ёц | здЯћЛЏb |
| 0.5% SDS | ||||||
| 0.01mol/L Tris(pH7.8) | ||||||
| ЕААзУИKc | 20mg/ml | -20ЁцЃЈШмгкЫЎЃЉ | 50ІЬg/ml | 0.005mol/L EDTA | 37ЁЋ56Ёц | ЮоаыдЄДІРэ |
| 0.5% SDS | ||||||
aЃКСДУЙЕААзУИЪЧДгСДЧђОњЃЈStreptomycesgriseusЃЉжаЗжРыЕНЕФвЛжжЫПАБЫсУИКЭЫсадЕААзУИЕФЛьКЯЮяЁЃ
bЃКздЯћЛЏПЩЯћГ§DNAУИКЭRNAУИЕФЮлШОЃЌОздЯћЛЏЕФСДУИЕААзУИЕФХфжЦЗНЗЈШчЯТЃКАбИУУИЕФЗлФЉШмНтгк10mmol./lTrisЁЄHCl(pH7.5)ЁЂ10mmol/l NaClжаЃЌХфГЩ20mg/mlХЈЖШЃЌгк37ЁцЮТг§1hЁЃОЯћЛЏЕФСДУЙЕААзУИЗжзАГЩаЁЗнЗХдкУмЗтЪдЙмжаЃЌБЃДц-20ЁцЁЃ
cЃКЕААзУИKЪЧвЛжжПнВнЕААзУИРрЕФИпЛюадЕААзУИЃЌДгСжВЎЪЯАзЩЋФюЧђОњЃЈTritirachium album LimberЃЉжаДПЛЏЕУЕНЁЃИУУИгаСНИіCa2+НсКЯЮЛЕуЃЌЫќУЧРыУИЕФЛюаджааФгавЛЖЈОрРыЃЌгыДпЛЏЛњРэВЂЮожБНгЙиЯЕЁЃШЛЖјЃЌШчЙћДгИУУИжаГ§ШЅCa2+ЃЌгЩгкГіЯждЖГЬЕФНсЙЙБфЛЏЃЌДпЛЏЛюадНЋЩЅЪЇ80%зѓгвЃЌЕЋЦфЪЃгрЛюадЭЈГЃвбзувдНЕНтдквЛАуЧщПіЯТЮлШОЫсжЦЦЗЕФЕААзжЪЁЃЫљвдЃЌЕААзУИKЯћЛЏЙ§ГЬжаЭЈГЃМгШыEDTAЃЈвдвжжЦвРРЕгкMg2+ЕФКЫЫсУИЕФзїгУЃЉЁЃЕЋЪЧЃЌШчЙћвЊЯћЛЏЖдЕААзУИKОпгаНЯЧПФЭадЕФЕААзЃЌШчНЧЕААзвЛРрЃЌдђПЩФмашвЊЪЙгУКЌга1mmol/l Ca2+ЖјВЛКЌEDTAЕФЛКГхвКЁЃдкЯћЛЏЭъБЯКѓЁЂДПЛЏКЫЫсЧАвЊМгШыEGTЃЈpH8.0ЃЉжСжеХЈЖШЮЊ2mmol/L,вдїЁКЯCa2+ЁЃ
3ЃЎЮоDNAУИЕФRNAУИ
НЋвШRNAУИЃЈRNAУИAЃЉШмгк10mmol/l TrisЁЄHCl(pH7.5)ЁЂ15mmol/l NaClжаЃЌХфГЩ10mg/mlЕФХЈЖШЃЌгк100ЁцМгШШ15minЃЌЛКТ§РфШДжСЪвЮТЃЌЗжзАГЩаЁЗнБЃДцгк-20ЁцЁЃ
ЫФЁЂГЃгУПЙЩњЫиШмвК
| ПЙЩњЫи | жќДцвКa | ЙЄзїХЈЖШ | ||
| ХЈЖШ | БЃДцЬѕМў | бЯНєаЭжЪСЃ | ЫЩГкаЭжЪСЃ | |
| АБмаЧрУЙЫи | 50mg/ml(ШмгкЫЎ) | -20Ёц | 20ІЬg/ml | 60ІЬg/ml |
| єШмаЧрУЙЫи | 50mg/ml(ШмгкЫЎ) | -20Ёц | 20ІЬg/ml | 60ІЬg/ml |
| ТШУЙЫи | 34mg/ml(ШмгкввДМ) | -20Ёц | 25ІЬg/ml | 170ІЬg/ml |
| ПЈФЧУЙЫи | 10mg/ml(ШмгкЫЎ) | -20Ёц | 10ІЬg/ml | 50ІЬg/ml |
| СДУЙЫи | 10mg/ml(ШмгкЫЎ) | -20Ёц | 10ІЬg/ml | 50ІЬg/ml |
| ЫФЛЗЫиb | 5mg/ml(ШмгкввДМ) | -20Ёц | 10ІЬg/ml | 50ІЬg/ml |
aЃКвдЫЎЮЊШмМСЕФПЙЩњЫижќДцвКЭЈЙ§0.22ІЬmТЫЦїЙ§ТЫГ§ОњЁЃвдввДМЮЊШмМСЕФПЙЩњЫиШмвКЮоаыГ§ОњДІРэЁЃЫљгаПЙЩњЫиШмвКОљгІЗХгкВЛЭИЙтЕФШнЦїБЃДцЁЃ
bЃКУОРызгЪЧЫФЛЗЫиЕФозПЙМСЃЌЫФЛЗЫиПЙадОњЕФЩИбЁгІЪЙгУВЛКЌУОбЮЕФХрбјЛљЃЈШчLBХрбјЛљЃЉЁЃ
ЮхЁЂГЃгУжќДцвКЕФХфжЦ
1ЃЎ30%БћЯЉѕЃАЗШмвК
ЁОХфжЦЗНЗЈЁП
НЋ29gБћЯЉѕЃАЗКЭ1g NЃЌNЁЏ-бЧМзЫЋБћЯЉѕЃАЗШмгкзмЬхЛ§ЮЊ60mlЕФЫЎжаЁЃМгШШжС37ЁцШмНтжЎЃЌВЙМгЫЎжСжеЬхЛ§ЮЊ100mlЁЃгУNalgeneТЫЦїЃЈ0.45ІЬmПзОЖЃЉЙ§ТЫГ§ОњЃЌВщжЄИУШмвКЕФpHжЕгІВЛДѓгк7.0ЃЌжУзиЩЋЦПжаБЃДцгкЪвЮТЁЃ
ЁОзЂвтЁП
БћЯЉѕЃАЗОпгаКмЧПЕФЩёОЖОадВЂПЩвдЭЈЙ§ЦЄЗєЮќЪеЃЌЦфзїгУОпРлЛ§адЁЃГЦСПБћЯЉѕЃАЗКЭбЧМзЫЋБћЯЉѕЃАЗЪБгІДїЪжЬзКЭУцОпЁЃПЩШЯЮЊОлБћЯЉѕЃАЗЮоЖОЃЌЕЋвВгІНїЩїВйзїЃЌвђЮЊЫќЛЙПЩФмЛсКЌгаЩйСПЮДОлКЯВФСЯЁЃ
вЛаЉМлИёНЯЕЭЕФБћЯЉѕЃАЗКЭЫЋБћЯЉѕЃАЗЭЈГЃКЌгавЛаЉН№ЪєРызгЃЌдкБћЯЉѕЃАЗжќДцвКжаМгШыДѓдМ0.2ЬхЛ§ЕФЕЅДВЛьКЯЪїжЌЃЈMB-1MallinckrodtЃЉЃЌНСАшЙ§вЙЃЌШЛКѓгУWhatman 1КХТЫжНЙ§ТЫвдДПЛЏжЎЁЃ
дкжќДцЦкМфЃЌБћЯЉѕЃАЗКЭЫЋБћЯЉѕЃАЗЛсЛКТ§зЊЛЏГЩБћЯЉѕЃКЭЫЋБћЯЉЫсЁЃ
2ЃЎ40%БћЯЉѕЃАЗ
ЁОХфжЦЗНЗЈЁП
Аб380gБћЯЉѕЃАЗЃЈDNAВтађМЖЃЉКЭ20g NЃЌNЁЏ-бЧМзЫЋБћЯЉѕЃАЗШмгкзмЬхЛ§ЮЊ600mlЕФеєСѓЫЎжаЁЃМЬајАДЩЯЪіХфжЦ30%БћЯЉѕЃАЗШмвКЕФЗНЗЈДІРэЃЌЕЋМгШШШмНтКѓгІвдеєСѓЫЎВЙзужСжеЬхЛ§ЮЊ1LЁЃ
ЁОзЂвтЁП
МћЩЯЪіХфжЦ30%БћЯЉѕЃАЗЕФЫЕУїЃЌ40%БћЯЉѕЃАЗШмвКгУгкDNAађСаВтЖЈЁЃ
3ЃЎЗХЯпОњЫиDШмвК
ЁОХфжЦЗНЗЈЁП
Аб20mgЗХЯпОњЫиDШмНтгк4ml 100%ввДМжаЃЌ1ЃК10ЯЁЪЭжќДцвКЃЌгУ100%ввДМзїПеАзЖдееЖСШЁOD440жЕЁЃЗХЯпОњЫиDЃЈЗжзгСПЮЊ1255ЃЉДПЦЗдкЫЎШмвКжаЕФФІЖћЯћЛЏЯЕЪ§ЮЊ21ЃЌ900ЃЌЙЪЖј1mg/mlЕФЗХЯпОњЫиDШмвКдк440nmДІЕФЮќЙтжЕЮЊ0.182ЃЌЗХЯпОњЫиDЕФжќДцвКгІЗХдкАќгаВЦЌЕФЪдЙмжаЃЌБЃДцгк-20ЁцЁЃ
ЁОзЂвтЁП
ЗХЯпОњЫиDЪЧжТЛћМСКЭжТАЉМСЃЌХфжЦИУШмвКЪББиаыДїЪжЬзВЂдкЭЈЗчГїФкВйзїЃЌЖјВЛФмдкПЊЗХдкЪЕбщзРУцЩЯНјааЃЌНїЗРЮќШывЉЗлЛђШУЦфНгДЅЕНблОІЛђЦЄЗєЁЃ
вЉГЇЬсЙЉЕФзїжЮСЦгУЭОЕФЗХЯпОњЫиDжЦЦЗГЃКЌгаЬЧЛђбЮЕШЬэМгМСЁЃжЛвЊЭЈЙ§ВтСПжќДцвКдк440nmВЈГЄДІЕФЙтЮќЪеШЗЖЈЗХЯпОњЫиDЕФХЈЖШЃЌетРржЦЦЗБуПЩгУгквжжЦздЩэв§ЕМзїгУЁЃ
4ЃЎ0.1mol/LЯймеШ§СзЫсЃЈATPЃЉШмвК
ЁОХфжЦЗНЗЈЁП
дк0.8mlЫЎжаШмНт60mgATP,гУ0.1mol/L NaOHЕїжСpHжЕжС7.0ЃЌгУеєСѓЫЎЖЈШн1mlЃЌЗжзАГЩаЁЗнБЃДцгк-70Ёц
5ЃЎ10mol/LввЫсѕЃШмвК
ЁОХфжЦЗНЗЈЁП
Аб770gввЫсѕЃШмНтгк800mlЫЎжаЃЌМгЫЎЖЈШнжС1LКѓЙ§ТЫГ§ОњЁЃ
6ЃЎ10%Й§СђЫсяЇШмвК
ЁОХфжЦЗНЗЈЁП
Аб1gЙ§СђЫсяЇШмНтгкжеСПЮЊ10mlЕФЫЎШмвКжаЃЌИУШмвКПЩдк4ЁцБЃДцЪ§жмЁЃ
7ЃЎBCIPШмвК
ЁОХфжЦЗНЗЈЁП
Аб0.5gЕФ5-фх-4-ТШ-3-пХпсСзЫсЖўФЦбЮЃЈBCIPЃЉШмНтгк10ml 100%ЕФЖўМзЛљМзѕЃАЗжаЃЌБЃДцгк4Ёц
8ЃЎ2ЁСBESЛКГхбЮШмвК
ЁОХфжЦЗНЗЈЁП
гУзмЬхЛ§90mlЕФеєСѓЫЎШмНт1.07gбЮШмвКBES[NЃЌN-ЫЋЃЈ2-єЧввЛљЃЉ-2-АБЛљввЛЧЫс]ЁЂ1.6g NaClКЭ0.027g Na2HPO4ЃЌЪвЮТЯТгУHClЕїНкЁЁИУШмвКЕФpHжЕжС6.96ЁЂШЛКѓМгШыеєСѓЫЎЖЈШнжС100mlЃЌгУ0.22ІЬmТЫЦїЙ§ТЫГ§ОњЃЌЗжзАГЩаЁЗнЃЌБЃДцгк-20ЁцЁЃ
9ЃЎ1mol/L CaCl2ШмвК
ЁОХфжЦЗНЗЈЁП
дк200mlеєСѓЫЎжаШмНт54gCaCl2ЁЄ6H2OЃЌгУ0.22ІЬmТЫЦїЙ§ТЫГ§ОњЃЌЗжзАГЩ10mlаЁЗнжќДцгк-20ЁцЁЃ
ЁОзЂвтЁП
жЦБИИаЪмЬЌЯИАћЪБЃЌШЁГівЛаЁЗнНтЖГВЂгУеєСѓЫЎЯЁЪЭжС100mlЃЌгУNalgeneТЫЦїЃЈ0.45ІЬmПзОЖЃЉЙ§ТЫГ§ОњЃЌШЛКѓжшРфжС0ЁцЁЃ
10ЃЎ2.5mol/L CaCl2ШмвК
ЁОХфжЦЗНЗЈЁП
дк20mlеєСѓЫЎжаШмНт13.5gCaCl2ЁЄ6H2OЃЌгУ0.22ІЬmТЫЦїЙ§ТЫГ§ОњЃЌЗжзАГЩ1mlаЁЗнжќДцгк-20ЁцЁЃ
11ЃЎ1mol/LЖўСђЫеЬЧДМЃЈDTTЃЉШмвК
ЁОХфжЦЗНЗЈЁП
гУ20ml 0.01mol/LввЫсФЦШмвКЃЈpH5.2ЃЉШмНт3.09g DTTЃЌЙ§ТЫГ§ОњКѓЗжзАГЩ1mlаЁЗнжќДцгк-20ЁцЁЃ
ЁОзЂвтЁП
DTTЛђКЌгаDTTЕФШмвКВЛФмНјааИпбЙДІРэЁЃ
12ЃЎЭббѕКЫмеШ§СзЫсЃЈdNTPЃЉШмвК
ЁОХфжЦЗНЗЈЁП
АбУПвЛжжdNTPШмНтгкЫЎжСХЈЖШИїЮЊ100mmol/LзѓгвЃЌгУЮЂСПвЦвКЦїЮќШЁ0.05mol/l TrisМюЗжБ№ЕїНкЁЁУПвЛdNTPШмвКЕФpHжЕ7.0ЃЈгУpHЪджНМьВтЃЉЃЌАбжаКЭКѓЕФУПжжdNTPШмвКИїШЁвЛЗнзїЪЪЕБЯЁЪЭЃЌдкЯТБэжаИјГіЕФВЈГЄЯТЖСШЁЙтУмЖШМЦЫуГіУПжжdNTPЕФЪЕМЪХЈЖШЃЌШЛКѓгУЫЎЯЁЪЭГЩжеХЈЖШЮЊ50mmol/LЕФdNTPЃЌЗжзАГЩаЁЗнжќДцгк-70ЁцЁЃ
| МюЛљ | ВЈГЄЃЈnmЃЉ | ЯћЛЏЯЕЪ§ЃЈІХЃЉ[L/ЃЈmolЁЄcmЃЉ] |
| A | 259 | 1.54ЁС104 |
| G | 253 | 1.37ЁС104 |
| C | 271 | 9.10ЁС103 |
| T | 260 | 7.40ЁС103 |
БШЩЋБЙтОЖЮЊ1cmЪБ,ЮќЙтЖШ=ІХM
13ЃЎ0.5mol/l EDTA(pH8.0)ШмвК
ЁОХфжЦЗНЗЈЁП
дк800mlЫЎжаМгШы186.1gЖўЫЎввЖўАЗЫФввЫсЖўФЦЃЈEDTA-NaЁЄ2H2OЃЉЃЌдкДХСІНСАшЦїЩЯОчСвНСАшЃЌгУNaOHЕїНкЁЁШмвКЕФpHжЕжС8.0ЃЈдМаш20g NaOHПХСЃЃЉШЛКѓЖЈШнжС1LЃЌЗжзАКѓИпбЙУ№ОњБИгУЁЃ
ЁОзЂвтЁП
EDTAЖўФЦбЮашМгШыNaOHНЋШмвКЕФpHжЕЕїжСНгНќ8.0ЃЌВХФмЭъШЋШмНтЁЃ
14ЃЎфхЛЏввЖЇЃЈ10mg/mlШмвКЃЉ
ЁОХфжЦЗНЗЈЁП
дк100mlЫЎжаМгШы1gфхЛЏввЖЇЃЌДХСІНСАшЪ§аЁЪБвдШЗБЃЦфЭъШЋШмНтЃЌШЛКѓгУТСВАќЙќШнЦїЛђзЊвЦжСзиЩЋЦПжаЃЌБЃДцгкЪвЮТЁЃ
ЁОзЂвтЁП
аЁаФЃКфхЛЏввЖЇЪЧЧПгеБфМСВЂгажаЖШЖОадЃЌЪЙгУКЌгаетжжШОСЯЕФШмвКЪБЮёБиДїЩЯЪжЬзЃЌГЦСПШОСЯЪБвЊДїУцежЁЃ
15ЃЎ2ЁСHEPESЛКГхбЮШмвК
ЁОХфжЦЗНЗЈЁП
гУзмСПЮЊ90mlЕФеєСѓЫЎШмНт1.6g NaClЁЂ0.074g KClЁЂ0.027g Na2PO4ЁЄ2H2OЁЂ0.2gЦЯОлЬЧКЭ1gHEPESЃЌгУ0.5mol/lNaOHЕїНкЁЁpHжЕжС7.05ЃЌдйгУеєСѓЫЎЖЈШнжС100mlЁЃгУ0.22ІЬmТЫЦїЙ§ТЫГ§ОњЃЌЗжзАГЩ5mlаЁЗнЃЌжќДцгк-20ЁцЁЃ
16ЃЎIPTGШмвК
ЁОХфжЦЗНЗЈЁП
IPTGЮЊвьБћЛљСђДњ-ІТ-D-АыШщЬЧмеЃЈЗжзгСПЮЊ238.3ЃЉЃЌдк8mlеєСѓЫЎжаШмНт2g IPTGКѓЃЌгУеєСѓЫЎЖЈШнжС10mlЃЌгУ0.22ІЬmТЫЦїЙ§ТЫГ§ОњЃЌЗжзАГЩ1mlаЁЗнжќДцгк-20ЁцЁЃ
17ЃЎ1mol/LввЫсУОШмвК
ЁОХфжЦЗНЗЈЁП
дк800mlЫЎжаШмНт214.46gЫФЫЎввЫсУОЃЌгУЫЎЖЈШнжС1LЙ§ТЫГ§ОњЁЃ
18ЃЎ1mol/L MgCl2ШмвК
ЁОХфжЦЗНЗЈЁП
дк800mlЫЎжаШмНт203.4gMgCl2ЁЄ6H2OЃЌгУЫЎЖЈШнжС1LЃЌЗжзАГЩаЁЗнВЂИпбЙУ№ОњБИгУЁЃ
ЁОзЂвтЁП
MgCl2МЋвзГБНтЃЌгІбЁЙКаЁЦПЃЈШч100gЃЉЪдМСЃЌЦєгУаТЦПКѓЮ№ГЄЦкДцЗХЁЃ
19ЃЎІТ-лЯЛљввДМЃЈBMEЃЉШмвК
ЁОХфжЦЗНЗЈЁП
вЛАуЕУЕНЕФЪЧ14.4mol/LШмвКЃЌгІзАдкзиЩЋЦПжаБЃДцгк4ЁцЁЃ
ЁОзЂвтЁП
BMEЛђКЌгаBMEЕФШмвКВЛФмИпбЙДІРэЁЃ
20ЃЎNBTШмвК
ЁОХфжЦЗНЗЈЁП
Аб0.5gТШЛЏЕЊРЖЫФпђШмНтгк10ml 70%ЕФЖўМзЛљМзѕЃАЗжаЃЌБЃДцгк4ЁцЁЃ
21ЃЎЗг/ТШЗТШмвК
ЁОХфжЦЗНЗЈЁП
АбЗгКЭТШЗТЕШЬхЛ§ЛьКЯКѓгУ0.1mol/L TrisЁЄHCl(pH7.6)ГщЬсМИДЮвдЦНКтетвЛЛьКЯЮяЃЌжУзиЩЋВЃСЇЦПжаЃЌЩЯУцИВИЧЕШЬхЛ§ЕФ0.01mol/l TrisЁЄHCl(pH7.6)вКВуЃЌБЃДцгк4ЁцЁЃ
ЁОзЂвтЁП
ЗгИЏЪДадКмЧПЃЌВЂПЩв§Ц№бЯжизЦЩЫЃЌВйзїЪБгІДїЪжЬзМАЗРЛЄОЕЃЌДЉЗРЛЄЗўЁЃЫљгаВйзїОљгІдкЛЏбЇЭЈЗчГїжаНјааЁЃгыЗгНгДЅЙ§ЕФВПЮЛЦЄЗєгІгУДѓСПЕФЫЎЧхЯДЃЌВЂгУЗЪдэКЭЫЎЯДЕгЃЌМЩгУввДМЁЃ
22ЃЎ10mmol/LБНМзЛљЛЧѕЃЗњЃЈPMSFЃЉШмвК
ЁОХфжЦЗНЗЈЁП
гУвьБћДМШмНтPMSFГЩ1.74mg/mlЃЈ10mmol/LЃЉЃЌЗжзАГЩаЁЗнжќДцгк-20ЁцЁЃШчгаБивЊПЩХфГЩХЈЖШИпДя17.4mg/mlЕФжќДцвКЃЈ100mmol/LЃЉЁЃ
ЁОзЂвтЁП
PMSFбЯжиЫ№КІКєЮќЕРеГФЄЁЂблОІМАЦЄЗєЃЌЮќШыЁЂЭЬНјЛђЭЈЙ§ЦЄЗєЮќЪеКѓгажТУќЮЃЯеЁЃвЛЕЉблОІЛђЦЄЗєНгДЅСЫPMSFЃЌгІСЂМДгУДѓСПЫЎГхЯДжЎЁЃЗВБЛPMSFЮлШОЕФвТЮягІгшЖЊЦњЁЃ
PMSFдкЫЎШмвКжаВЛЮШЖЈЁЃгІдкЪЙгУЧАДгжќДцвКжаЯжгУЯжМггкСбНтЛКГхвКжаЁЃPMSFдкЫЎШмвКжаЕФЛюадЩЅЪЇЫйТЪЫцpHжЕЕФЩ§ИпЖјМгПьЃЌЧв25ЁцЕФЪЇЛюЫйТЪИпгк4ЁцЁЃpHжЕЮЊ8.0ЪБЃЌ20ІЬmmol/l PMSFЫЎШмвКЕФАыЪйЦкДѓдМЮЊ85minЃЌетБэУїНЋPMSFШмвКЕїНкЁЁЮЊМюадЃЈpH>8.6ЃЉВЂдкЪвЮТЗХжУЪ§аЁЪБКѓЃЌПЩАВШЋЕигшвдЖЊЦњЁЃ
23ЃЎСзЫсбЮЛКГхШмвКЃЈPBSЃЉШмвК
ЁОХфжЦЗНЗЈЁП
дк800mlеєСѓЫЎжаШмНт8gNaClЁЂ0.2g KClЁЂ1.44g Na2HPO4КЭ0.24g KH2PO4,гУHClЕїНкЁЁШмвКЕФpHжЕжС7.4МгЫЎЖЈШнжС1LЃЌдк15lbf/in2(1034ЁС105Pa)ИпбЙЯТеєЦјУ№Оњ20minЁЃБЃДцгкЪвЮТЁЃ
24ЃЎ1mol/LввЫсМиЃЈpH7.5ЃЉШмвК
ЁОХфжЦЗНЗЈЁП
НЋ9.82gввЫсМиШмНтгк90mlДПЫЎжаЃЌгУ2mol/LввЫсЕїНкЁЁpHжЕжС7.5КѓМгШыДПЫЎЖЈШнЕН1LЃЌБЃДцгк-20ЁцЁЃ
25ЃЎввЫсМиШмвКЃЈгУгкМюСбНтЃЉ
ЁОХфжЦЗНЗЈЁП
дк60ml 5mol/LввЫсМиШмвКжаМгШы11.5mlБљввЫсКЭ28.5mlЫЎЃЌМДГЩМиХЈЖШЮЊ3mol/LЖјввЫсИљХЈЖШЮЊ5mol/LЕФШмвКЁЃ
26ЃЎ3mol/LввЫсФЦЃЈpH5.2КЭpH7.0ЃЉШмвК
ЁОХфжЦЗНЗЈЁП
дк80mlЫЎжаШмНт408.1gШ§ЫЎввЫсФЦЃЌгУБљввЫсЕїНкЁЁpHжЕжС5.2ЛђгУЯЁввЫсЕїНкЁЁpHжЕжС7.0ЃЌМгЫЎЖЈШнЕН1LЃЌЗжзАКѓИпбЙУ№ОњЁЃ
27ЃЎ5mol/L NaClШмвК
ЁОХфжЦЗНЗЈЁП
дк800mlЫЎжаШмНт292.2gNaClМгЫЎЖЈШнжС1LЃЌЗжзАКѓИпбЙУ№ОњЁЃ
28ЃЎ10%ЪЎЖўЭщЛљСђЫсФЦЃЈSDSЃЉШмвК
ЁОХфжЦЗНЗЈЁП
дк900mlЫЎжаШмНт100gЕчгОМЖSDSЃЌМгШШжС68ЁцжњШмЃЌМгШыМИЕЮХЈбЮЫсЕїНкЁЁШмвКЕФpHжЕжС7.2ЃЌМгЫЎЖЈШнжС1LЃЌЗжзАБИгУЁЃ
ЁОзЂвтЁП
SDSЕФЮЂЯИОЇСЃвзРЉЩЂЃЌвђДЫГЦСПЪБвЊДїУцежЃЌГЦСПЭъБЯКѓвЊЧхГ§ВаСєдкГЦСПЙЄзїЧјКЭЬьЦНЩЯЕФSDSЃЌ10%SDSШмвКЮоаыУ№ОњЁЃ
29ЃЎ20ЁСSSCШмвК
ЁОХфжЦЗНЗЈЁП
дк800mlЫЎжаШмНт175.3gNaClКЭ88.2gФћУЪЫсФЦЃЌМгШыЪ§ЕЮ10mol/l NaOHШмвКЕїНкЁЁpHжЕжС7.0ЃЌМгЫЎЖЈШнжС1LЃЌЗжзАКѓИпбЙУ№ОњЁЃ
30ЃЎ20ЁСSSPEШмвК
ЁОХфжЦЗНЗЈЁП
дк800mlЫЎжаШмНт17.5gNaClЁЂ27.6g NaH2PO4ЁЄH2OКЭ7.4g EDTAЃЌгУNaOHШмвКЕїНкЁЁpHжЕжС7.4ЃЈдМаш6.5ml 10ml/L NaOHЃЉЃЌМгЫЎЖЈШнжС1LЃЌЗжзАКѓИпбЙУ№ОњЁЃ
31ЃЎ100%Ш§ТШввЫсШмвК
ЁОХфжЦЗНЗЈЁП
дкзАга500g TCAЕФЦПжаМгШы227mlЫЎЃЌаЮГЩЕФШмвККЌга100%ЃЈM/VЃЉTCAЁЃ
32ЃЎ1mol/L TrisШмвК
ЁОХфжЦЗНЗЈЁП
дк800mlЫЎжаШмНт121.91gTrisМюЃЌМгШыХЈHClЕїНкЁЁpHжЕжСЫљашжЕЁЃ
pHЁЁHCl
7.4 70ml
7.6 60ml
8.0 42ml
гІЪЙШмвКРфжСЪвЮТКѓЗНПЩзюКѓЕїЖЈpHжЕЃЌМгЫЎЖЈШнжС1LЃЌЗжзАКѓИпбЙУ№ОњЁЃ
ЁОзЂвтЁП
Шч1mol/LШмвКГЪЯжЛЦЩЋЃЌгІгшЖЊЦњВЂжУБИжЪСПИќКУЕФTrisЁЃ
ОЁЙмЖржжРраЭЕФЕчМЋОљВЛФмзМШЗВтСПTrisШмвКЕФpHжЕЃЌЕЋШдПЩЯђДѓЖрЪ§ГЇЩЬЙКЕУКЯЪЪЕФЕчМЋЁЃ
TrisШмвКЕФpHжЕвђЮТЖШЖјвьЃЌЮТЖШУПЩ§Ип1ЁцЃЌpHжЕДѓдМНЕЕЭ0.03ИіЕЅЮЛЁЃР§ШчЃК0.05mol/LЕФШмвКдк5ЁцЁЂ25ЁцЁЂКЭ37ЁцЪБЕФpHжЕЗжБ№ЮЊ9.5ЁЂ8.9КЭ8.6ЁЃ
33ЃЎTrisЛКГхбЮШмвКЃЈTBSЃЉЃЈ25mmol/l TrisЃЉ
ЁОХфжЦЗНЗЈЁП
дк800mlеєСѓЫЎжаШмНт8gNaClЁЂ0.2g KClКЭ3g TrisМюЃЌМгШы0.015gЗгВЂгУHClЕїжСpHжЕжС7.4ЃЌгУеєСѓЫЎЖЈШнжС1LЃЌЗжзАКѓдк151bf/in2(1.034ЁС105Pa)ИпбЙЯТеєЦћУ№Оњ20minЃЌгкЪвЮТБЃДцЁЃ
34ЃЎX-galШмвК
ЁОХфжЦЗНЗЈЁП
X-galЮЊ5-фх-4-ТШ-3-пХпс-ІТ-DАыШщЬЧмеЁЃгУЖўЛљМзѕЃАЗШмНтX-galХфжЦГЩЕФ20mg/mlЕФжќДцвКЁЃБЃДцгквЛВЃСЇЙмЛђОлБћЯЉЙмжаЃЌзАгаX-galШмвКЕФЪдЙмаыгУТСВЗтЙќвдЗРвђЪмЙтееЖјБЛЦЦЛЕЃЌВЂгІжќДцгк-20ЁцЁЃX-galШмвКЮоаыЙ§ТЫГ§ОњЁЃ
дгНЛЪдбщжагУгкНЕЕЭБГОАЕФЗтБеМС
| ЪдМС | гУЭО |
| DenhardtЪдМС | NorthernдгНЛ |
| ЪЙгУRNAЬНеыЕФдгНЛ | |
| ЕЅПНБДађСаЕФSouthernдгНЛ | |
| НЋDNAЙЬЖЈгкФсСњФЄЩЯЕФдгНЛ | |
| DenhardtЪдМСЭЈГЃХфжЦ50ЁСжќДцвКЃЌЙ§ТЫКѓБЃДцгк-20ЁцЁЃПЩНЋИУжќДцвК10БЖЯЁЪЭгкдЄдгНЛвКЃЈГЃЮЊКЌга0.5%SDSКЭ100ІЬg/mlОБфадБЛДђЖЯЕФійОЋDNAЕФ6ЁСSSCЛђ6ЁСSSPEЃЉжаЁЃ50ЁСDenhardtвКжаКЌ5gОлесЬЧЃЈFicoll,400аЭЃЌPharmaciaЃЉЁЂ5gОлввЯЉпСПЉЭщЭЊКЭ5gХЃбЊЧхАзЕААзЃЈзщЗжVЁБSigmalЃЉЃЌМгЫЎжСжеЬхЛ§ЮЊ500mlЁЃ | |
| BLOTTO | Grunstein-HognessдгНЛ |
| Benton-DavisдгНЛ | |
| Г§ЕЅПНБДађСаSouthernдгНЛвдЭтЕФЫљгаSouthernдгНЛ | |
| АпЕугЁМЃ | |
| 1ЁСBLOTTЃЈХЃШщзЊвЦММЪѕгХЛЏвКЃЌBovine Lacto Transfer Technique OptimizerЃЉ,ЪЧКЌ5%НКжЌФЬЗлКЭ0.02%ЕўЕЊФЦЕФЫЎШмвКЃЌгІБЃДцгк4ЁцЁЃЪЙгУЧАПЩгУдЄдгНЛвКЯЁЪЭ25БЖЁЃBLOTTOВЛгІгыИпХЈЖШЕФSDSВЂгУЃЌвђЮЊКѓепЛсЕМжТХЃФЬжаЕААзжЪЮіГіЁЃШчЙћдгНЛБГОАВЛКЯвЊЧѓЃЌПЩдкдгНЛвКжаМгШыNP-40жСжеХЈЖШЮЊ1%ЁЃBLOTTOВЛФмгУзїNorthernдгНЛЕФЗтБеМСЃЌвђЮЊетвЛЗтБеМСжаПЩФмКЌгаRNAУИЃЌЦфЛюаджЎИпЪЙШЫЮоЗЈНгЪмЁЃ | |
| зЂвтЃКЕўЕЊФЦгаЖОадЃЌШЁгУЪБашДїЪжЬзаЁаФВйзїЁЃКЌЕўЕЊФЦЕФШмвКгІгшУїШЗБъМЧЁЃ | |
| ИЮЫи | SouthernдгНЛ |
| дЮЛдгНЛ | |
| ИЮЫиЃЈSigma H-7005ЃЌДгжэжаЬсШЁЕФЖўМЖВњЦЗЛђЯрЕБЕШМЖЕФВњЦЗЃЉгУ4ЁСSSPEЛђ4ЁСSSCШмНтХфжЦГЩ50mg/mlЕФХЈЖШЃЌБЃДцгк4ЁцЁЃИЮЫидкКЌгаЦЯОлЬЧСђЫсѕЅЕФдгНЛвКжагУзїЗтБеМСЕФХЈЖШЮЊ500ІЬg/mlЃЌдкВЛКЌЦЯОлЬЧСђЫсѕЅЕФдгНЛвКжаЕФХЈЖШЮЊ50ІЬg/mlЁЃ | |
| ОБфадВЂБЛДђЖЯЕФійОЋDNA | southernКЭNorthernдгНЛ |
| АбійгуОЋзгDNAЃЈSigma,Ђѓ,бЮФЦЃЉШмНтгкЫЎХфжЦГЩ10mg/mlЕФХЈЖШЃЌБивЊЪБгкЪвЮТДХСІНСАш2ЁЋ4hжњШмЁЃАбШмвКжаNaClЕФХЈЖШЕїжС0.1mol/LЃЌВЂгУЗгКЭЗг/ТШЗТИїГщЬсвЛДЮЃЌЛиЪеЫЎЯрЁЃКЯDNAШмвКПьЫйЭЈ17КХЦЄЯТзЂЩфеыЭЗ12ДЮЃЌвдМєЧаDNAЁЃМгШы2БЖЬхЛ§гУБљдЄРфЕФввДМГСЕэDNAЁЃРыаФЛиЪеDNAВЂжиШмгкЫЎЃЌХфжЦГЩ10mg/mlЕФХЈЖШЃЌВтЖЈШмвКЕФOD260жЕВЂМЦЫуГіОЋШЗЕФDNAХЈЖШЃЌШЛКѓжѓЗа10minЃЌЗжзАГЩаЁЗнБЃДцгк-20ЁцЁЃЪЙгУЧАжУЗаЫЎдЁжаМгШШ5minЃЌШЛКѓбИЫйдкБљдЁжажшРфЁЃдЄдгНЛвКжагІКЌга100ІЬg/mlОБфадВЂБЛДђЖЯЕФійгуОЋзгDNA | |
СљЁЂГЃгУФ§НКЕФММЪѕВЮЪ§
1ЃЎЦЯОлЬЧФ§НКЕФФГаЉММЪѕЪ§Он
| жжРр | ИЩПХСЃжБОЖЃЈІЬЃЉ | ЗжзгСПЗжМЖЗЖЮЇ | ДВЬхЛ§КСЩ§/ПЫИЩЗжзгЩИ | ЕУЫЎжЕ | ШмеЭзюЩйЦНКтЪБМфЃЈhЃЉ | жљЭЗбЙСІЃЈkPaЃЉ(2.5cmжБОЖжљ) | ||
| ыФМАЧђаЮЕААзжЪ | ЦЯОлЬЧЃЈЯпадЗжзгЃЉ | ЪвЮТ | ЗаЫЎдЁ | |||||
| Sephadex G-10 | 40ЁЋ 120 | ЁЋ700 | ЁЋ700 | 2ЁЋ 3 | 1.0ЁР0.1 | 3 | 1 | ЁЁ |
| Sephadex G-10 | 40ЁЋ 120 | ЁЋ1500 | 1500 | 2.5ЁЋ3.5 | 1.5ЁР3.5 | 3 | 1 | ЁЁ |
| Sephadex G-25 | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ДжМЖ | 100ЁЋ300 (Ёж5ЁЋ100ФП) | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| жаМЖ | 50ЁЋ150 (Ёж100ЁЋ200ФП) | 1,000ЁЋ 5,000 | 100ЁЋ 5,000 | 4ЁЋ6 | 1.5ЁР0.2 | 6 | 2 | |
| ЯИМЖ | 20ЁЋ800(Ёж200ЁЋ400ФП) | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ГЌЯИ | 10ЁЋ40 | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| Sephadex G-50 | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ДжМЖ | 100ЁЋ200 | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| жаМЖ | 50ЁЋ150 | 1,500ЁЋ | 500ЁЋ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ЯИМЖ | 20ЁЋ80 | 30,000 | 10,000 | 9ЁЋ11 | 5.0ЁР0.3 | 6 | 2 | |
| ГЌЯИ | 10ЁЋ40 | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| Sephadex G-75 | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ЁЁ | 40ЁЋ120 | 3,000ЁЋ | 1,000ЁЋ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ГЌЯИ | 10ЁЋ40 | 70,000 | 950,000 | 12ЁЋ15 | 7.5ЁР0.5 | 24 | 3 | 3.92ЁЋ15.86 |
| Sephadex G-100 | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ЁЁ | 40ЁЋ120 | 4,000ЁЋ | 1,000ЁЋ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ГЌЯИ | 10ЁЋ40 | 1,500,000 | 150,000 | 15ЁЋ20 | 10.0ЁР1.0 | 48 | 5 | 2.35ЁЋ9.41 |
| Sephadex G-150 | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ЁЁ | 40ЁЋ120 | 5,000ЁЋ | 1,000ЁЋ | 20ЁЋ30 | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ГЌЯИ | 10ЁЋ40 | 400,000 | 150,000 | 18ЁЋ22 | 15.0ЁР1.5 | 72 | 5 | 0.88ЁЋ3.53 |
| Sephadex G-200 | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ЁЁ | 40ЁЋ120 | 5000ЁЋ | 1000ЁЋ | 30ЁЋ40 | ЁЁ | ЁЁ | ЁЁ | ЁЁ |
| ЁЁ | 10ЁЋ40 | 800,000 | 200,000 | 20ЁЋ25 | 20.0ЁР2.0 | 72 | 5 | 0.39ЁЋ1.57 |
2.ОлБћЯЉѕЃАЗФ§НКЕФММЪѕЪ§Он
| аЭКХ | ХХзшЕФЯТЯо (ЗжзгСП) | ЗжМЖЗжРыЗЖЮЇ (ЗжзгСП) | ХђеЭКѓЕФДВЬхЛ§(ml/gИЩФ§НК) | ХђеЭЫљашзюЩйЪБМф(ЪвЮТ,h) |
| Bio-gel-P-2 | 1,600 | 200ЁЋ2,000 | 3.8 | 2ЁЋ4 |
| Bio-gel-P-4 | 3,600 | 500ЁЋ4,000 | 5.8 | 2ЁЋ4 |
| Bio-gel-P-6 | 4,600 | 1,000ЁЋ5,000 | 8.8 | 2ЁЋ4 |
| Bio-gel-P-10 | 10,000 | 5,000ЁЋ17,000 | 12.4 | 2ЁЋ4 |
| Bio-gel-P-30 | 30,000 | 20,000ЁЋ50,000 | 14.9 | 10ЁЋ12 |
| Bio-gel-P-60 | 60,000 | 30,000ЁЋ70,000 | 19.0 | 10ЁЋ12 |
| Bio-gel-P-100 | 100,000 | 40,000ЁЋ100,000 | 19.0 | 24 |
| Bio-gel-P-150 | 150,000 | 50,000~150,000 | 24.0 | 24 |
| Bio-gel-P-200 | 200,000 | 80,000ЁЋ200,000 | 34.0 | 48 |
| Bio-gel-P-300 | 300,000 | 100ЁЋ400,000 | 40.0 | 48 |
3ЃЎЧэжЌЬЧФ§НКЕФММЪѕЪ§Он
| аЭКХ | ЧэжЌЬЧКЌСП %ЃЈW/WЃЉ | ХХзшЕФЯТЯо ЃЈЗжзгСПЃЉ | ЗжМЖЗжРыЕФЗЖЮЇЃЈЗжзгСПЃЉ | ЩњВњГЇМв |
| Sepharose 4B | 4 | ЁЁ | 0.3ЁС106ЁЋ3ЁС106 | Pharmacia |
| Sepharose 2B | 2 | ЁЁ | 2ЁС106ЁЋ25ЁС106 | |
| Sagavac 10 | 10 | 2.5ЁС105 | 1ЁС104ЁЋ2.5ЁС105 | Seravac |
| Sagavac 8 | 8 | 7ЁС105 | 2.5ЁС104ЁЋ7ЁС105 | |
| Sagavac 6 | 6 | 2ЁС106 | 5ЁС104ЁЋ2ЁС106 | |
| Sagavac 4 | 4 | 15ЁС106 | 2ЁС105ЁЋ15ЁС106 | |
| Sagavac 2 | 2 | 150ЁС106 | 5ЁС105ЁЋ15ЁС107 | |
| Bio-gel A-0.5M | 10 | 0.5ЁС106 | <1ЁС104ЁЋ0.5ЁС106 | Bio-Rad |
| Bio-gel A-1.5M | 8 | 1.5ЁС106 | <1ЁС104ЁЋ1.5ЁС106 | |
| Bio-gel A-5M | 6 | 5ЁС106 | 1ЁС104ЁЋ5ЁС106 | |
| Bio-gel A-15M | 4 | 15ЁС106 | 4ЁС104ЁЋ15ЁС106 | |
| Bio-gel A-50M | 2 | 50ЁС106 | 1ЁС105ЁЋ50ЁС106 | |
| Bio-gel A-150M | 1 | 150ЁС106 | 1ЁС106ЁЋ150ЁС106 |
4ЃЎИїДІФ§НКЫљдЪаэЕФзюДѓВйзїбЙ
| Ф§НК | зюДѓОВЫЎбЙЃЈkPaЃЉ |
| Sephadex | ЁЁ |
| G-10 | 9.8 |
| G-15 | 9.8 |
| G-25 | 9.8 |
| G-50 | 9.8 |
| G-75 | 4.9 |
5ЃЎЧэжЌЬЧФ§НКХЈЖШгыЯпадDNAЗжБцЗЖЮЇ
| Ф§НКХЈЖШЃЈ%ЃЉ | ЯпадDNAГЄЖШЃЈbpЃЉ |
| 0.5 | 1000ЁЋ30000 |
| 0.7 | 800ЁЋ12000 |
| 1.0 | 500ЁЋ10000 |
| 1.2 | 400ЁЋ7000 |
| 1.5 | 200ЁЋ3000 |
| 2.0 | 50ЁЋ2000 |
6ЃЎШОСЯдкБфадОлБћЯЉѕЃАЗФ§НКжаЕФЧЈвЦЫйЖШ
| Ф§НКХЈЖШЃЈ%ЃЉ | фхЗгРЖ | ЖўМзБНЧрFF |
| 5ЃЎ0 | 35bp | 140bp |
| 6ЃЎ0 | 26bp | 106bp |
| 8ЃЎ0 | 19bp | 75bp |
| 10ЃЎ0 | 12bp | 55bp |
| 20ЃЎ0 | 8bp | 28bp |
7ЃЎШОСЯдкЗЧБфадОлБћЯЉѕЃАЗФ§НКжаЕФЧЈвЦЫйЖШ
| Ф§НКХЈЖШЃЈ%ЃЉ | фхЗгРЖ | ЖўМзБНЧрFF |
| 3.5 | 100bp | 460bp |
| 5.0 | 65bp | 260bp |
| 8.0 | 45bp | 160bp |
| 12.0 | 20bp | 70bp |
| 15.0 | 15bp | 50bp |
| 20.0 | 12bp | 45bp |
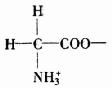
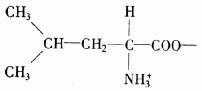
ЦпЁЂАБЛљЫсЕФЬиад
| АБЛљЫсУћГЦ | Ш§зжФИЫѕаД | ЕЅзжФИЫѕаД | жЪСП | ВрСДЕчРыЕФpHaжЕ | НсЙЙЪН |
| БћАБЫсЃЈalanineЃЉ | Ala | A | 89.09 | ЁЁ |
|
| ОЋАБЫсЃЈarginineЃЉ | Arg | R | 174.2 | 12.48 |
|
| ЬьЖЌѕЃАБЃЈasparagineЃЉ | Asn | N | 132.1 | ЁЁ |
|
| ЬьЖЌАБЫсЃЈaspartic acidЃЉ | Asp | D | 133.1 | 3.86 |
|
| АыызАБЫсЃЈsysteineЃЉ | Cys | C | 121.12 | ЁЁ |
|
| ЙШАБѕЃАЗЃЈglutamineЃЉ | Gln | Q | 146.15 | ЁЁ |
|
| ЙШАБЫсЃЈglutamic acidЃЉ | Glu | E | 147.13 | 4.25 |
|
| ИЪАБЫсЃЈglycineЃЉ | Gly | G | 75.07 | ЁЁ |
|
| зщАБЫсЃЈhistidineЃЉ | His | H | 155.16 | 6.0 |
|
| вьССАБЫсЃЈisoleucineЃЉ | lle | I | 131.17 | ЁЁ |
|
| ССАБЫсЃЈleucineЃЉ | Leu | L | 131.17 | ЁЁ |
|
| РЕАБЫсЃЈlycineЃЉ | Lys | K | 146.19 | ЁЁ |
|
| МзСђАБЫсЃЈmethionineЃЉ | Met | M | 149.21 | ЁЁ |
|
| БНБћАБЫсЃЈphenylanalineЃЉ | Phe | P | 165.19 | ЁЁ |
|
| ИЌАБЫсЃЈprolineЃЉ | Pro | P | 115.13 | ЁЁ |
|
| ЫПАБЫсЃЈserineЃЉ | Ser | S | 105.06 | ЁЁ |
|
| ЫеАБЫс(threonine) | Thr | T | 119.12 | ЁЁ |
|
| ЩЋАБЫсЃЈtryptophanЃЉ | Trp | W | 204.22 | ЁЁ | |
| РвАБЫсЃЈtyrosineЃЉ | Tyr | Y | 181.19 | 10.07 |
|
| чгАБЫсЃЈvalineЃЉ | Val | P | 117.15 | ЁЁ |
|
АЫЁЂвХДЋУмТы
УмТызгЕФЕкЖўЮЛ
| УмТызгЕФЕквЛЮЛЃЈ5ЁЏЖЫЃЉ | ЁЁ | U | C | A | G | ЁЁ | УмТызгЕФЕкШ§ЮЛЃЈ3ЖЫЁЏЃЉ | ||||
| U | UUU | Phe | UCU | Ser | UAU | Tyr | UGU | Gys | U | ||
| UUC | Phe | UCC | Ser | UAC | Tyr | UGG | Gys | C | |||
| UUA | Leu | UCA | Ser | UAA | жежЙЃЈєїЪЏЃЉ | UGA | жежЙЃЈШщАзЃЉ | A | |||
| UUG | Leu | UGG | Ser | UAG | жежЙЃЈчњчъЃЉ | UGG | Trp | G | |||
| C | CUU | Leu | CCU | Pro | CAU | His | CGA | Arg | U | ||
| CUC | Leu | CCC | Pro | CAC | His | CGC | Arg | C | |||
| CUA | Leu | CCA | Pro | CAA | Gln | CGA | Arg | A | |||
| CUG | Leu | CCG | Pro | CAG | Gln | CGC | Arg | G | |||
| A | AUU | Ile | ACU | Thr | AAU | Asn | AGU | Ser | U | ||
| AUC | Ile | ACC | Thr | AAC | Asn | AGC | Ser | C | |||
| AUA | Ile | ACA | Thr | AAA | Lys | AGA | Arg | A | |||
| AUG | Met | ACG | Thr | AAG | Lys | AGC | Arg | G | |||
| G | GUU | Val | GCU | Ala | GAU | Asp | GGU | Gly | U | ||
| GUC | Val | GCC | Ala | GAC | Asp | GGC | Gly | C | |||
| GUA | Val | GCA | Ala | GAA | Glu | GGA | Gly | A | |||
| GUG | Val | GCG | Ala | GAG | Glu | GGG | Gly | G | |||
ОХЁЂГЃгУЫсМюММЪѕВЮЪ§
1ЃЎ
| ШмжЪ | ЗжзгЪН | ЗжзгСП | mol/L | g/L | жиСПЃЈ%ЃЉ | БШжи | ХфжЦmol/LШмвКЕФМгШыСПЃЈml/LЃЉ |
| БљввЫс | CH3COOH | 60.05 | 17.40 | 1045 | 99.5 | 1.050 | 57.5 |
| ввЫс | ЁЁ | 60.05 | 6.27 | 376 | 36 | 1.045 | 159.5 |
| МзЫс | HCOOH | 46.02 | 23.40 | 1080 | 90 | 1.200 | 42.7 |
| бЮЫс | HCl | 36.50 | 11.60 | 424 | 36 | 1.180 | 86.2 |
| ЁЁ | ЁЁ | ЁЁ | 2.90 | 105 | 10 | 1.050 | 344.8 |
| ЯѕЫс | HNO3 | 63.02 | 15.99 | 1008 | 71 | 1.420 | 62.5 |
| ЁЁ | ЁЁ | ЁЁ | 14.90 | 938 | 67 | 1.400 | 67.1 |
| ЁЁ | ЁЁ | ЁЁ | 13.30 | 837 | 61 | 1.370 | 75.2 |
| ИпТШЫс | HclO3 | 100.50 | 11.65 | 1172 | 70 | 1.670 | 85.8 |
| ЁЁ | ЁЁ | ЁЁ | 9.20 | 923 | 60 | 1.540 | 108.7 |
| СзЫс | H2PO4 | 80.00 | 18.10 | 1445 | 85 | 1.700 | 55.2 |
| СђЫс | H2PЃрO4 | 98.10 | 18.00 | 1776 | 96 | 1.840 | 55.6 |
| ЧтбѕЛЏяЇ | NH4OH | 35.00 | 14.80 | 251 | 28 | 0.898 | 67.6 |
| ЧтбѕЛЏМи | KOH | 56.10 | 13.50 | 757 | 50 | 1.520 | 74.1 |
| ЁЁ | ЁЁ | ЁЁ | 1.94 | 109 | 10 | 1.090 | 515.5 |
| ЧтбѕЛЏФЦ | NaOH | 40.00 | 19.10 | 763 | 50 | 1.530 | 52.4 |
| ЁЁ | ЁЁ | ЁЁ | 2.75 | 111 | 10 | 1.110 | 363.4 |
2ЃЎИїжжХЈЖШЕФЫсМюжќДцвКЕФНќЫЦpHжЕ
| ШмжЪ | 1Na | 0.1Na | 0.01Na | 0.001Na |
| ввЫс | 0.40 | 2.90 | 3.40 | 3.90 |
| бЮЫс | 0.10 | 1.07 | 2.02 | 3.01 |
| СђЫс | 0.30 | 1.20 | 2.10 | ЁЁ |
| ФћУЪЫс | ЁЁ | 2.10 | 2.60 | ЁЁ |
| ЧтбѕЛЏяЇ | 11.80 | 11.30 | 10.80 | 10.30 |
| ЧтбѕЛЏФЦ | 14.05 | 13.07 | 12.12 | 11.13 |
| ЬМЫсЧтФЦ | ЁЁ | 8.40 | ЁЁ | ЁЁ |
| ЬМЫсФЦ | ЁЁ | 11.50 | 11.00 | ЁЁ |
J a.NЮЊЙтСПХЈЖШ[1NЁжЃЈ1mol/LЃЉЁСРызгМлЪ§]ЁЃ
ЪЎЁЂЗХЩфадКЫЫиЪ§Он
1ЃЎЗХЩфадКЫЫиЫЅБфБэ
| 3H | 35S | 32P | 125I | 131I | |||||
| ЪБМф(Фъ) | ЪЃгрЛюад(%) | ЪБМф(Фъ) | ЪЃгрЛюад(%) | ЪБМф(Фъ) | ЪЃгрЛюад(%) | ЪБМф(Фъ) | ЪЃгрЛюад(%) | ЪБМф(Фъ) | ЪЃгрЛюад(%) |
| 1 | 94.5 | 2 | 98.4 | 1 | 95.3 | 4 | 95.5 | 0.2 | 98.3 |
| 2 | 89.3 | 5 | 96.1 | 2 | 90.8 | 8 | 91.2 | 0.4 | 96.6 |
| 3 | 84.4 | 10 | 92.3 | 3 | 86.5 | 12 | 87.1 | 0.6 | 95.0 |
| 4 | 79.8 | 15 | 88.7 | 4 | 82.5 | 16 | 83.1 | 1.0 | 91.8 |
| 5 | 75.4 | 20 | 85.3 | 5 | 78.5 | 20 | 79.4 | 1.6 | 87.2 |
| 6 | 71.3 | 25 | 82.0 | 6 | 74.8 | 24 | 75.8 | 2.3 | 81.2 |
| 7 | 67.4 | 31 | 78.1 | 7 | 71.2 | 28 | 72.4 | 3.1 | 76.7 |
| 8 | 63.7 | 37 | 74.5 | 8 | 67.8 | 32 | 69.1 | 4.0 | 71.0 |
| 9 | 60.2 | 43 | 71.0 | 9 | 64.7 | 36 | 66.0 | 5.0 | 65.2 |
| 10 | 56.9 | 50 | 67.0 | 10 | 61.2 | 40 | 63.0 | 6.1 | 59.3 |
| 11 | 53.8 | 57 | 63.6 | 11 | 58.7 | 44 | 60.2 | 7.3 | 53.4 |
| 12 | 50.9 | 65 | 59.6 | 12 | 55.9 | 48 | 57.4 | 8.1 | 50.0 |
| 12.3 | 50.0 | 73 | 56.0 | 13 | 53.2 | 52 | 54.8 | ЁЁ | ЁЁ |
| ЁЁ | ЁЁ | 81 | 52.5 | 14 | 50.7 | 56 | 52.4 | ЁЁ | ЁЁ |
| ЁЁ | ЁЁ | 87.1 | 50.0 | 14.3 | 50.0 | 60 | 50.0 | ЁЁ | ЁЁ |
2.ЗХЩфадВтЖЈЕЅЮЛ
| ЕЅЮЛ | ЖЈвх | ЛЛЫу |
| ЮќЪеЗХЩфЯпМССПЃЈРЕУradЃЉ | 100ЖћИё/ПЫЃЈЕчРыЗјЩфДЋИјЕЅЮЛжЪСПЮяжЪЕФФмСПЃЉ | 0.87rad=1r |
| ТзЧйЃЈrЃЉ | ЪЙ1ПЫПеЦјВњЩњ1.6ЁС1012РызгЖдЕФXЛђІУ-ЩфЯпЕФееЩфМССП | r/0.87=1rad |
| ОгРяЃЈCiЃЉ | УПУыЗХЩфадЫЅБф3.7ЁС1010ИідзгЕФСП | 1Ci=103mCi=106ІЬCi |
| КСОгЃЈmCiЃЉ | ЧЇЗжжЎвЛОгРя | 1mCi=10-3Ci=103ІЬCi |
| ЮЂОгЃЈІЬCiЃЉ | АйЭђЗжжЎвЛОгРяЃЈУПЗжжгЫЅБф2.2ЁС106ДЮЃЉ | 1ІЬCi=10-6Ci=10-3MCi |
| ВЎПЫРГЖћЃЈBqЃЉ | УПУыЫЅБф1ИідзгЕФСП | 1Bq=3.7ЁС10-10Ci |
| ЧЇВЎПЫРГЖћЃЈkBqЃЉ | ЁЁ | 1kBq=103Bq |
| АйЭђВЎПЫРГЖћЃЈMBqЃЉ | ЁЁ | 1MBq=106Bq |
| езВЎПЫРГЖћЃЈGBqЃЉ | ЁЁ | 1GBq=109Bq |
| УПЗжжгЫЅБфЪ§ЃЈdpmЃЉ | УПЗжжгЫЅБфЕФдзгЪ§ | 2.2ЁС106dpm=1ІЬCi |
| УПЗжжгМЦЪ§ЃЈcpmЃЉ | ВтСПвЧВтГіУПЗжжгІТСЃзгЪ§ | Cpm=dpmЁСМЦЪ§ЦїаЇТЪ |
ЪЎвЛЁЂдзгСП
| ЗћКХ | дзгађЪ§ | дзгСП | |
| яЙЃЈactiniumЃЉ | Ac | 89 | 227.02 |
| ТСЃЈaluminiumЃЉ | Al | 13 | 26.98 |
| ябЃЈamericiumЃЉ | Am | 95 | (243) |
| ЬрЃЈantimonyЃЉ | Sb | 51 | 121.75 |
| ыВЃЈargonЃЉ | Ar | 18 | 39.94 |
| ЩщЃЈarsenicЃЉ | As | 33 | 74.92 |
| эСЃЈastatineЃЉ | At | 85 | (210) |
| БЕЃЈbariumЃЉ | Ba | 56 | 137.33 |
| яТЃЈberkeliumЃЉ | Bk | 97 | (247) |
| юыЃЈberylliumЃЉ | Be | 4 | 9.01 |
| ющЃЈbismuthЃЉ | Bi | 83 | 208.98 |
| Х№ЃЈboronЃЉ | B | 5 | 10.81 |
| фхЃЈbromineЃЉ | Br | 35 | 79.90 |
| ягЃЈcadmiumЃЉ | Cd | 48 | 112.41 |
| ИЦЃЈcalciumЃЉ | Ca | 20 | 40.08 |
| яДЃЈcaliforniumЃЉ | Cf | 98 | (251) |
| ЬМЃЈcarbonЃЉ | C | 6 | 12.01 |
| юцЃЈceriumЃЉ | Ce | 58 | 140.12 |
| яЄЃЈcesiumЃЉ | Cs | 55 | 132.90 |
| ТШЃЈchlorineЃЉ | Cl | 17 | 35.45 |
| ИѕЃЈchromiumЃЉ | Cr | 24 | 51.99 |
| юмЃЈcobaltЃЉ | Co | 27 | 58.93 |
| ЭЃЈcopperЃЉ | Cu | 29 | 63.54 |
| яИЃЈcuriumЃЉ | Cm | 96 | (247) |
| ясЃЈdysprosiumЃЉ | Dy | 66 | 162.50 |
| яЭЃЈeinsteiniumЃЉ | Es | 99 | (252) |
| юяЃЈerbiumЃЉ | Er | 68 | 167.26 |
| ю№ЃЈeuroqiumЃЉ | Eu | 63 | 151.96 |
| яаЃЈfermiumЃЉ | Fm | 100 | (257) |
| ЗњЃЈfluorineЃЉ | F | 9 | 18.99 |
| юеЃЈfranciumЃЉ | Fr | 87 | (223) |
| юХЃЈgadoliniumЃЉ | Gd | 64 | 157.52 |
| яиЃЈgaliumЃЉ | Ga | 31 | 69.72 |
| ерЃЈgermaniumЃЉ | Ge | 32 | 72.59 |
| Н№ЃЈgoldЃЉ | Au | 79 | 196.96 |
| юўЃЈhafniumЃЉ | Hf | 72 | 178.49 |
| КЄЃЈheliumЃЉ | He | 2 | 4.00 |
| юиЃЈholmiumЃЉ | Ho | 67 | 164.93 |
| ЧтЃЈhydrogenЃЉ | H | 1 | 1.00 |
| юїЃЈindiumЃЉ | In | 49 | 114.82 |
| ЕтЃЈiodineЃЉ | I | 53 | 126.90 |
| вПЃЈiridiumЃЉ | Ir | 77 | 192.22 |
| ЬњЃЈironЃЉ | Fe | 26 | 55.84 |
| ыДЃЈkryptonЃЉ | Kr | 36 | 83.80 |
| ячЃЈlanthanumЃЉ | La | 57 | 139.90 |
| яЉЃЈLawrenciumЃЉ | Lr | 103 | (260) |
| ЧІЃЈleadЃЉ | Pb | 82 | 207.2 |
| яЎЃЈlithiumЃЉ | Li | 3 | 6.94 |
| яхЃЈlutetiumЃЉ | Lu | 71 | 174.96 |
| УОЃЈMagnesiumЃЉ | Mg | 12 | 24.30 |
| УЬЃЈmanganseЃЉ | Mn | 25 | 54.93 |
| юЭЃЈmendeleviumЃЉ | Md | 101 | (258) |
| ЙЏЃЈmolybdenumЃЉ | Hg | 80 | 200.59 |
| ютЃЈmolybdenumЃЉ | Mo | 42 | 95.94 |
| юЯЃЈneodymiumЃЉ | Nd | 60 | 144.24 |
| ФЪЃЈneonЃЉ | Ne | 10 | 20.17 |
| яеЃЈneptuniumЃЉ | Np | 93 | 237.04 |
| ФјЃЈnickelЃЉ | Ni | 28 | 58.69 |
| юъЃЈniobiumЃЉ | Nb | 41 | 92.00 |
| ЕЊЃЈnitrogenЃЉ | N | 7 | 14.00 |
| яЛЃЈnobeliumЃЉ | No | 102 | (259) |
| яАЃЈosmiumЃЉ | Os | 76 | 190.2 |
| бѕЃЈoxygenЃЉ | O | 8 | 15.99 |
| юйЃЈpalladiumЃЉ | Pd | 46 | 106.42 |
| СзЃЈphosphorusЃЉ | P | 15 | 30.94 |
| ВЌЃЈplatiumЃЉ | Pt | 78 | 195.08 |
| юаЃЈpiutoniumЃЉ | Pu | 94 | (244) |
| юЧЃЈpoloniumЃЉ | Po | 84 | (209) |
| МиЃЈpotassiumЃЉ | K | 19 | 39.09 |
| яшЃЈpraseodymiumЃЉ | Pr | 59 | 140.90 |
| ювЃЈpromethiumЃЉ | Pm | 61 | (145) |
| яфЃЈprotactiniumЃЉ | Pa | 91 | 231.03 |
| РиЃЈradiumЃЉ | Ra | 88 | 226.02 |
| ыБЃЈradonЃЉ | Rn | 86 | (222) |
| яЊЃЈrheniumЃЉ | Re | 75 | 186.20 |
| ююЃЈrhodiumЃЉ | Rh | 45 | 102.90 |
| яЈЃЈrubidiumЃЉ | Rb | 37 | 85.46 |
| юЩЃЈrutheniumЃЉ | Ru | 44 | 101.07 |
| юЬЃЈsamariumЃЉ | Sm | 62 | 150.36 |
| южЃЈscandiumЃЉ | Sc | 21 | 44.95 |
| ЮјЃЈsilliconЃЉ | Se | 34 | 78.96 |
| ЙшЃЈsilliconЃЉ | Si | 14 | 28.08 |
| вјЃЈsliverЃЉ | Ag | 47 | 107.86 |
| ФЦЃЈsodiumЃЉ | Na | 11 | 22.98 |
| яШЃЈstrontiumЃЉ | Sr | 38 | 87.62 |
| СђЃЈsulfurЃЉ | S | 16 | 32.06 |
| юуЃЈtantalumЃЉ | Ta | 73 | 180.94 |
| яНЃЈtechnetiumЃЉ | Tc | 43 | (98) |
| экЃЈtelluriumЃЉ | Te | 52 | 127.60 |
| яЋЃЈterbiumЃЉ | Tb | 65 | 158.92 |
| юшЃЈthalliumЃЉ | Tl | 81 | 204.38 |
| юЪЃЈthoriumЃЉ | Th | 90 | 232.03 |
| Ю§ЃЈtinЃЉ | Sn | 50 | 118.69 |
| юћЃЈthuliumЃЉ | Tm | 69 | 168.93 |
| юбЃЈtitaniumЃЉ | Ti | 22 | 47.88 |
| ЮйЃЈtungstenЃЉ | W | 74 | 183.85 |
| unhilhexium | (Unh) | 106 | (263) |
| unnilpentium | (Unp) | 105 | (262) |
| unnilquadium | (Unq) | 104 | (261) |
| unnilseptium | (Uns) | 107 | (262) |
| гЫЃЈuraniumЃЉ | U | 92 | 238.02 |
| ЗАЃЈvanadiumЃЉ | V | 23 | 50.94 |
| ыЏЃЈxenonЃЉ | Xe | 54 | 131.29 |
| язЃЈytterbiumЃЉ | Yb | 70 | 173.04 |
| юЦЃЈyttriumЃЉ | Y | 39 | 88.90 |
| аПЃЈzincЃЉ | Zn | 30 | 65.38 |
| яЏЃЈzirconiumЃЉ | Zn | 40 | 91.22 |
дВРЈКХжаЕФЪ§зжЪЧИУдЊЫизюЮШЖЈЕФЭЌЮЛЫиЕФжЪСПЪ§ЁЃ
ЃЈЮтПЕЃЉ
-
ЁЖЪЕгУУтвпЯИАћгыКЫЫсЁЗ жаЕФЯрЙиеТНкЃК
ЁЁЁЁ
ЁЁЁЁВЮПМЮФЯз
ИНТМ
ЁЁЁЁИНТМвЛЁЁУтвпЯИАћЛЏбЇГЃгУЪдМСНщЩм
ЁЁЁЁИНТМЖўЁЁдЮЛдгНЛзщжЏЛЏбЇГЃгУЪдМСМАДІРэ
ЁЁЁЁИНТМШ§ЁЁШЋбЊЯИАћХрбјШОЩЋЬхММЪѕГЃгУЪдМСХфжЦ
ЁЁЁЁИНТМЫФЁЁЪЕбщЪвГЃгУММЪѕВЮЪ§зЪСЯЃЈЕБЧАвГЃЉ
ЁЁЁЁБОЪщГЃгУЫѕаДДЪ
ЁЁЁОЭъЁП